Кровь традиционно воспринимается как жизненно важная ткань, необходимая для поддержания функций организма, однако в биотехнологии она рассматривается прежде всего как сложное и ценное сырьё. Плазма, форменные элементы, факторы свертывания и содержащиеся в крови биоактивные молекулы становятся объектами тонкой инженерной работы. Задача биотехнолога здесь не только в том, чтобы «извлечь пользу» из крови, но и в том, чтобы превратить её в безопасный, стандартизированный и предсказуемый продукт для пациента. Это означает очистку от вирусов и бактерий, снижение риска иммунных осложнений, создание рекомбинантных аналогов белков крови, а также разработку новых форм носителей для лекарств на основе эритроцитов и тромбоцитов.
Кровь как биосырьё: плазма и клетки
С точки зрения биотехнологии кровь — это многокомпонентная система, где каждая фракция обладает своим функциональным потенциалом. Плазма, представляющая собой водный раствор белков (альбумин, иммуноглобулины, факторы свертывания), служит исходным материалом для получения лекарственных препаратов и для структурирования биоматериалов. Эритроциты интересны как кислородтранспортные носители и естественные нанокапсулы для доставки лекарств. Тромбоциты и фибриноген используются как основа для регенеративных гелей и матриксов, а лейкоциты — как источник биоактивных пептидов и клеточных платформ.
Базовым технологическим шагом является фракционирование цельной крови. В лабораторных и промышленных условиях кровь разделяют с помощью центрифугирования и сепарации при строго контролируемых режимах скорости и температуры. Это позволяет выделить плазму, эритроцитарную массу, тромбоцитарный концентрат и промежуточные фракции. Корректное и бережное разделение критически важно: повреждённые клетки и денатурированные белки ухудшают качество конечных препаратов и могут повышать риск осложнений у реципиента. Поэтому режимы фракционирования подбирают таким образом, чтобы сохранить функциональность белков и клеток и обеспечить воспроизводимость партий.
Типичная схема получения продуктов крови из донорской крови показана на схеме ниже.
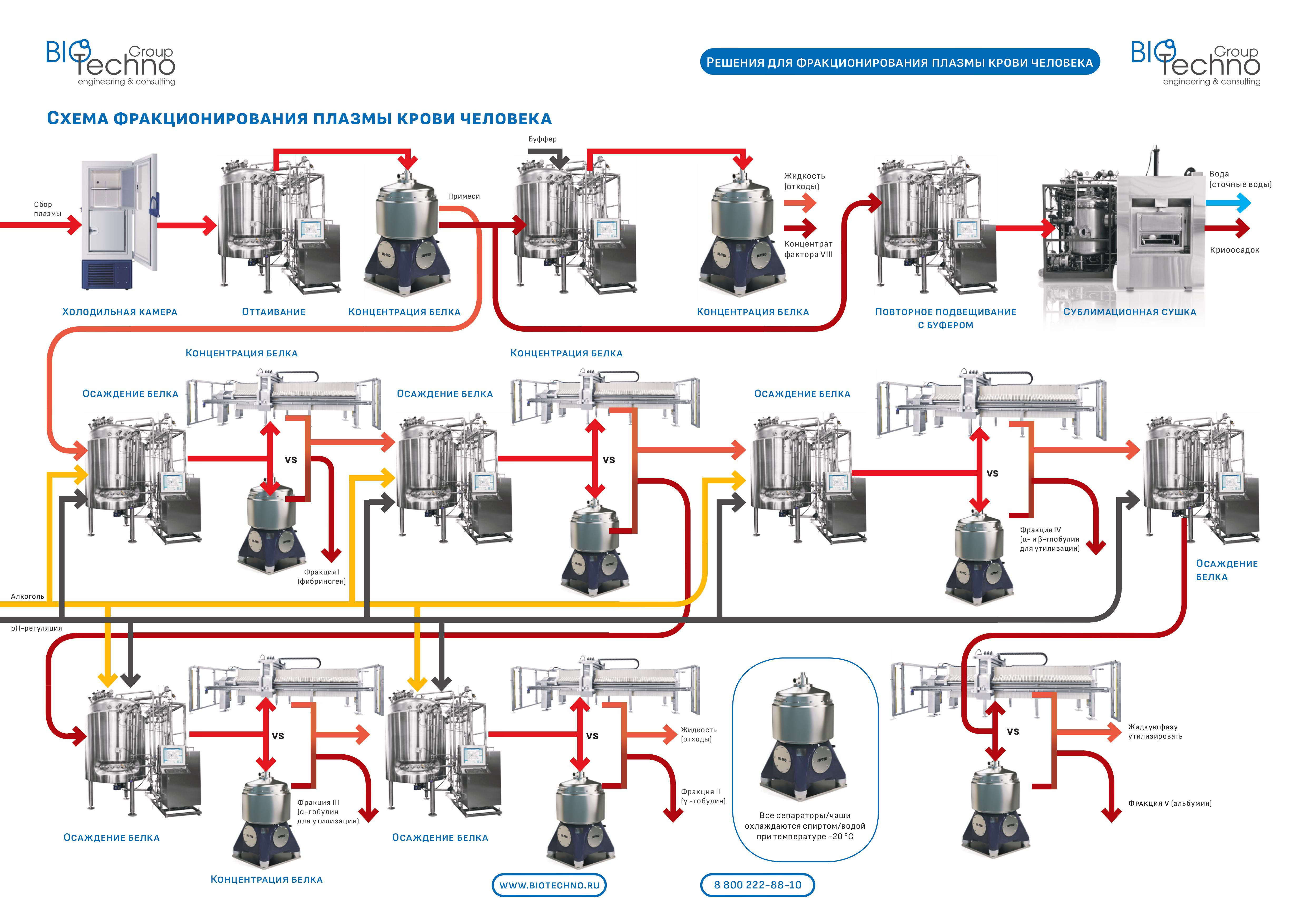
Компания Биотехно предлагает сепараторы для получения продуктов крови. Главное преимущество - мощное и строго контролируемое охлаждение, что критически важно для осаждения целевых белков из плазмы.

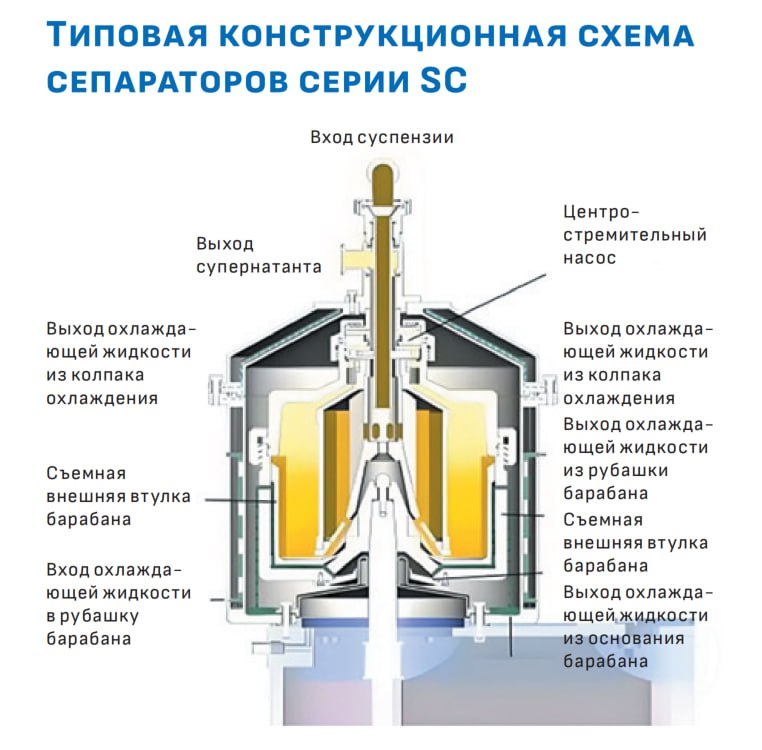
Вирусная безопасность и патоген‑редукция
Одним из ключевых вызовов при работе с донорской кровью всегда была опасность передачи инфекций. Даже при тщательном опросе и скрининге доноров сохраняется риск того, что в крови присутствуют вирусы или другие патогены, не выявленные на этапе тестирования. Биотехнология решает эту проблему за счёт внедрения многоступенчатых методик вирусной инактивации и патоген‑редукции, которые встроены в технологическую схему подготовки плазмы и клеточных компонентов.
Один из наиболее известных подходов — фотохимическая вирусинактивация. В плазму или тромбоцитарный концентрат вводят фотосенсибилизатор, взаимодействующий с нуклеиновыми кислотами вирусов, после чего материал подвергают контролируемому облучению светом определённого спектра. Вирусные геномы повреждаются и теряют способность к репликации, в то время как функциональность белков плазмы, при правильно подобранных режимах, в значительной степени сохраняется. Такой метод позволяет существенно снизить риск передачи широкого спектра вирусов, включая новые или малоизученные.
Дополнительно применяются технологии обработки растворителями и детергентами, разрушающие липидную оболочку вирусов, а также пастеризация и обработка сухим жаром для отдельных препаратов. Важно, что эти процедуры являются не «ручными» манипуляциями, а стандартизированными биотехнологическими процессами с чётко заданными параметрами времени, температуры, концентраций реагентов и последующего контроля качества. По сути, кровь перестаёт быть «непредсказуемым» биоматериалом и проходит через фильтр биотехнологии, которая отсеивает потенциально опасные агенты ещё до того, как продукт попадёт к пациенту.
Микробиологическая безопасность и контроль качества
Помимо вирусов, существенную угрозу при переливании представляют бактерии. Они могут попадать в кровь на этапе забора, хранения или переработки и приводить к тяжёлым септическим реакциям у реципиента. Биотехнологический подход к этой проблеме сочетает профилактику и строгий аналитический контроль.
На этапе заготовки используются закрытые системы, позволяющие минимизировать контакт крови с окружающей средой. В ряде случаев применяется отбрасывание «первой порции» крови, в которой выше вероятность присутствия бактерий с поверхности кожи. Во многих центрах переливания вводится микробиологический мониторинг партий компонентов крови: часть единиц отправляют на посев или экспресс‑тесты, оценивая наличие бактериальной контаминации ещё до выдачи продукта клинике.
Параллельно действуют регламенты, основанные на принципах надлежащей производственной практики. Контролируется чистота воздуха, состояние оборудования, частота и качество дезинфекции. Таким образом, биотехнология в работе с кровью — это не только химические и физические процедуры, но и целая культура производства, где соблюдение стандартов напрямую влияет на безопасность реципиента.
Оптимизация совместимости: от групп крови до иммуногенетики
Совместимость донорской крови с организмом реципиента — ещё один слой задачи, где биотехнология играет заметную роль. На базовом уровне всё начинается с определения группы крови по системе ABO и резус‑фактора. Здесь используются разработанные тест‑системы и автоматизированные анализаторы, снижающие вероятность ошибки и обеспечивающие быстрое и точное типирование.
Однако при сложных вмешательствах, таких как трансплантация гемопоэтических стволовых клеток, этого уже недостаточно. Важным становится соответствие по системе HLA — комплексу гистосовместимости. Для его оценки применяют молекулярно‑генетические методы: полимеразную цепную реакцию, высокоразрешающее секвенирование, гибридизационные панели. Это уже чистая биотехнология, где анализ генетической информации позволяет подобрать донора так, чтобы риск отторжения и тяжёлых иммунных осложнений был минимален.
Отдельным направлением является лейкодеплеция — удаление лейкоцитов из компонентов крови. Лейкофильтрация снижает риск лихорадочных негемолитических реакций, уменьшает вероятность формирования антител к HLA и некоторых других иммунных осложнений, а также дополнительно уменьшает риск передачи определённых вирусов, ассоциированных с лейкоцитами. Здесь снова объединяются инженерные решения (фильтрующие системы) и биологические знания о том, какие клетки и в каком объёме нужно удалить, чтобы минимизировать риск для пациента.
Рекомбинантные белки: когда кровь заменяется биореактором
Важнейшая тенденция последних десятилетий заключается в постепенном отказе от ряда плазменных препаратов в пользу рекомбинантных аналогов. Если раньше факторы свертывания для пациентов с гемофилией практически полностью получали из донорской плазмы, то теперь существенная часть таких препаратов производится с помощью генно‑инженерных клеточных линий.
Клетки млекопитающих (чаще всего линии CHO или HEK) модифицируют так, чтобы они экспрессировали человеческий фактор VIII, IX или другие белки.

Эти клетки выращиваются в биореакторах при строго контролируемых условиях: поддерживаются оптимальные температура, pH, концентрация растворённого кислорода и питательных веществ.
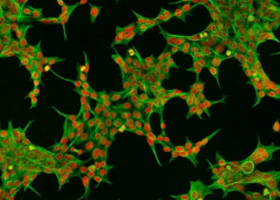
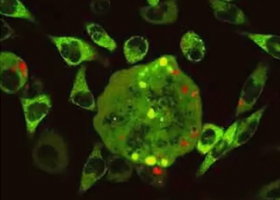
После культивирования белок очищают, концентрируют и подвергают многоэтапному контролю качества. В результате получается продукт, по структуре и функции близкий к природному, но не связанный ни с донорской кровью, ни с её инфекционными рисками.
Для пациента это означает дополнительный уровень безопасности: рекомбинантный препарат не несёт в себе потенциальных вирусных частиц и не зависит от ограниченности донорского ресурса. Для биотехнологии же это пример того, как традиционно «кровяной» продукт может быть полностью перенесён в область клеточных и молекулярных технологий.
Эритроциты как носители лекарств
Эритроциты, основная задача которых в организме — переносить кислород, в биотехнологии рассматриваются как удобные биологические контейнеры. Их мембрана и длительное время циркуляции в кровотоке делают их привлекательными носителями для лекарственных веществ.
Существуют технологии инкапсулирования лекарств внутрь эритроцитов: клетки подвергают осмотическим, электрическим или химическим воздействиям, временно повышая проницаемость мембраны. Внутрь попадает препарат, после чего мембрана восстанавливает свою целостность. Такие «нагруженные» эритроциты можно возвращать пациенту. Они распределяются по организму, сохраняя при этом часть естественных свойств и постепенно высвобождая активное вещество. Это позволяет уменьшить токсичность, увеличить продолжительность действия препарата и в перспективе — настроить его доставку к определённым органам или системам.
Тромбоциты, фибрин и регенеративные материалы
Тромбоциты и фибриноген, помимо своей естественной роли в свертывании крови, стали основой для целого направления регенеративной медицины. Концентраты, обогащённые тромбоцитами (PRP, PRF), получают из аутологичной крови пациента с помощью контролируемого центрифугирования. В результате формируется плазма или гель с высоким содержанием тромбоцитов и фибрина, насыщенный факторами роста.
Такие препараты используют в стоматологии, ортопедии, травматологии и пластической хирургии для стимуляции заживления костных и мягких тканей. Биотехнологический вклад здесь состоит в стандартизации протоколов получения, подборе режимов центрифугирования, разработке стерильных наборов и контейнеров, а также изучении профиля высвобождения факторов роста.
На следующем уровне развития находятся гибридные материалы, где компоненты крови сочетаются с неорганическими и полимерными матрицами. Фибрин или плазма могут служить основой для формирования композитов с гидроксиапатитом, пригодных для заполнения костных дефектов. Биоматериал, сформированный частично из крови пациента, лучше интегрируется с окружающими тканями, а контролируемая структура и состав позволяют управлять скоростью его резорбции и замещения собственной костной тканью.
Кровь и новые биоматериалы
Интересным направлением стала разработка материалов, в которых кровь участвует как активная среда сборки структуры. Существуют концепции, где синтетические пептиды добавляют в кровь пациента, и в результате их взаимодействия формируется материал, напоминающий природную регенеративную гематому. Такой материал можно использовать как имплантат или заготовку для трёхмерной печати, а его свойства во многом определяются именно взаимодействием с кровяными компонентами.
Такие решения показывают, что кровь в биотехнологии — это не только источник белков и клеток, но и динамическая среда, способная самоорганизовываться в сложные структуры под действием заданных сигналов. Это открывает путь к персонализированным имплантатам, сформированным непосредственно из биологического материала конкретного пациента.
Заключение
Кровь в биотехнологии — это одновременно сырьё, платформа и среда для сложных инженерных решений. На уровне безопасности биотехнологические процессы очищают её от вирусов и бактерий, снижая риск для реципиента. На уровне совместимости они помогают точнее подбирать доноров и модифицировать компоненты крови, уменьшая иммунные осложнения. На уровне продуктов они позволяют создавать рекомбинантные аналоги плазменных белков, разрабатывать «умные» носители на основе эритроцитов и тромбоцитов и проектировать новые биоматериалы для регенерации тканей.

 Хранение культур
Хранение культур  Подготовка сред
Подготовка сред  Лабораторная ферментация
Лабораторная ферментация  Пилотная ферментация
Пилотная ферментация  Вспомогательное оборудование
Вспомогательное оборудование  Комплектующие
Комплектующие  Лабораторное оборудование
Лабораторное оборудование  Программное обеспечение
Программное обеспечение  Промышленная ферментация
Промышленная ферментация  Выделение и очистка продукта
Выделение и очистка продукта  Сепарация и центрифугирование
Сепарация и центрифугирование  Лиофильная сушка
Лиофильная сушка  Ферментёры
Ферментёры  Биореакторы
Биореакторы  Cепарация
Cепарация  Фильтрация
Фильтрация  Cушилки
Cушилки  Одноразовые биотехнологические решения
Одноразовые биотехнологические решения  Решения для контроля контаминации в чистых помещениях
Решения для контроля контаминации в чистых помещениях  Фармацевтические изоляторы и решения для транспортировки материалов
Фармацевтические изоляторы и решения для транспортировки материалов  Хроматографические системы
Хроматографические системы